Глава 17. Физико-химические основы процесса горения
17.1. Общие сведения о горении и взрыве

Горение - это интенсивные химические окислительные реакции, которые сопровождаются выделением теплоты и свечением. Горение может возникнуть только при одновременном наличии трех условий: присутствии горючего вещества, окислителя и источника (импульса) воспламенения.
Горючие вещества - любые органические вещества и материалы, большинство металлов в свободном виде, многие минералы, сера, оксид углерода, водород, фосфор и т.д.
В качестве окислителя может быть не только кислород, но и многие химические соединения - бертолетова соль, перхлораты, нитросоединения, пероксид натрия, азотная кислота, хлор, озон и др.
Импульсами воспламенения могут быть открытые, или светящиеся источники - пламя, раскаленные поверхности, лучистая энергия, искры, а также скрытые (несветящиеся) - трение, удар, адиабатическое сжатие, экзотермическая реакция и т.д. Например, температура пламени спички составляет 750-8600С, тления сигареты - 700-750, пламени древесной лучины - 850-10000С.
В некоторых случаях при горении конденсированных систем (твердых, жидких веществ или их смесей) пламя может и не возникать, т.е. происходит беспламенное горение, или тление.
Для того чтобы прервать горение, необходимо нарушить условия его возникновения и поддержания. Обычно для тушения используют нарушение двух основных условий устойчивого состояния горения - понижение температуры и режим движения газов.
В зависимости от агрегатного состояния исходного вещества и продуктов горения различают гомогенное горение, гетерогенное горение и горение взрывчатых веществ.
При гомогенном горении исходные вещества и продукты горения находятся в одинаковом агрегатном состоянии. Это:
- горение газовых смесей (природного газа, водорода, оксида углерода и других веществ с окислителем - обычно кислородом воздуха);
- горение негазифицирующихся конденсированных веществ, например, термитов (смеси алюминия с оксидами различных металлов);
- изотермическое горение - распространение цепной разветвленной реакции в газовой смеси без значительного разогрева.
При гетерогенном горении исходные вещества находятся в разных агрегатных состояниях. К основным технологическим процессам гетерогенного горения относятся горение угля, металлов, сжигание жидких топлив в топках, двигателях внутреннего сгорания и т.д.
Горение взрывчатых веществ сопровождается переходом вещества из конденсированного в газовое состояние. При этом на поверхности раздела фаз происходит сложный физико-химический процесс, при котором в результате химической реакции выделяются теплота и горючие газы, догорающие в зоне горения на некотором расстоянии от поверхности.
Движение пламени по газовой смеси называется распространением пламени. В зависимости от скорости распространения пламени горение может быть диффузионным (несколько метров в секунду), дефлаграционным или взрывным (десятки и сотни метров в секунду) и детонационным (тысячи метров в секунду).
При горении химически неоднородных горючих систем, т.е. систем, в которых горючее вещество и воздух не перемешаны и имеют поверхности раздела (твердые материалы и жидкости; струи паров и газов, поступающих в воздух), время диффузии кислорода к горючему веществу несоизмеримо больше времени, необходимого для протекания химической реакции. В этом случае процесс протекает в диффузионной области. Такое горение называют диффузионным. Все пожары представляют собой диффузионное горение.
Если время физической стадии перемешивания горючих веществ с окислителем несоизмеримо меньше времени протекания самой химической реакции, то такой процесс горения называют кинетическим, и он может протекать в виде взрыва.
Если продолжительность химической реакции соизмерима со временем физической стадии, то горение протекает в промежуточной области.
Пространство, в котором сгорают пары и газы, называют пламенем или факелом.
Для дефлаграционного горения характерна передача теплоты от слоя к слою, а пламя, возникающее в нагретой с активными радикалами и продуктами реакции смеси, перемещается в направлении исходной горючей смеси. Это объясняется тем, что пламя выделяет непрерывный поток теплоты и химически активных частиц, в результате чего фронт пламени перемещается в сторону горючей смеси.
Скорость горения горючих веществ в смеси с воздухом для предельных углеводородов составляет 0,32-0,4 м/с, водорода - 2,7 м/с. При таких скоростях распространения пламени образование ударной волны перед фронтом пламени не происходит.
При достижении скоростей распространения пламени, составляющих десятки и сотни метров в секунду, но не превышающих скорость распространения звука в данной среде (300-320 м/с), происходит взрывное горение.
Взрыв по ГОСТ 12.1.010 - быстрое превращение вещества (взрывное горение), сопровождающееся выделением энергии и образованием сжатых газов, способных производить работу.
При взрывном горении продукты горения могут нагреваться до 1500-3000°С, а давление в закрытых системах увеличиваться до 0,6-0,9 МПа.
В условиях промышленного производства под взрывом следует понимать быстрое неуправляемое высвобождение энергии, которое вызывает ударную волну, движущуюся на некотором расстоянии от источника. Источниками энергии при взрыве могут быть как химические, так и физические процессы.
В реальных промышленных условиях происходят локальные взрывы («хлопки») парогазовых выбросов из технологических систем, сопровождающиеся сильным звуковым эффектом. При этом создается избыточное давление, которое в определенных условиях может оказывать разрушающее действие.
К наибольшему разрушающему эффекту приводят локальные взрывы веществ, характеризующиеся высокими скоростями распространения пламени при сравнительно небольшой массе горючего вещества. Взрыв может быть вызван детонацией конденсированного взрывчатого вещества, быстрым сгоранием воспламеняющегося облака газа, внезапным разрушением сосуда со сжатым газом или перегретой жидкостью, смешиванием перегретых твердых веществ (расплава) с холодными жидкостями и т.д. Источником химического взрыва являются быстропротекающие экзотермические реакции взаимодействия горючих веществ с окислителями или термического разложения нестабильных соединений.
Взрыв, как правило, сопровождается возникновением ударной волны, т.е. интенсивным ростом давления в окружающей среде.
Ударная волна обладает разрушительной способностью, если избыточное давление в ней превышает 15 кПа. Она распространяется в газовой среде перед фронтом пламени со скоростью звука - 330 м/с. Разрушающее давление порядка 30 кПа достигается при скорости распространения пламени 150-200 м/с.
При определенных условиях взрывное горение может перейти в детонационный процесс, при котором скорость распространения пламени превышает скорость звука и достигает 1-5 км/с.
Детонация - это процесс химического превращения системы окислитель - восстановитель, представляющий собой совокупность ударной волны, распространяющейся с постоянной скоростью и превышающей скорость звука, и следующей за фронтом зоны химических превращений исходных веществ. Химическая энергия, выделяющаяся в детонационной волне, подпитывает ударную волну, не давая ей затухать. Пиковое давление, создаваемое при детонации, достигает 200 кПа. Большинство промышленных зданий разрушается при давлениях 25-30 кПа при внешних взрывах и 20-25 кПа - при внутренних.
При детонационном режиме горения парогазовоздушной смеси большая часть энергии взрыва переходит в ударную волну; при взрывном горении переход энергии в ударную волну составляет около 30%.
В результате взаимодействия горючего вещества с окислителем образуются продукты сгорания, состав которых зависит от исходных веществ и условий реакции горения.
При полном сгорании органических соединений образуются, как правило, углекислый газ, диоксид серы, вода, азот, а при сгорании неорганических соединений - оксиды. Состав продуктов неполного сгорания горючих веществ сложен и разнообразен. Это могут быть такие горючие вещества, как сажа, водород, угарный газ, метан; атомарный водород и кислород; различные радикалы - ОН, СН и др. Продуктами неполного сгорания могут быть также более сложные вещества - оксиды азота, спирты, альдегиды, кетоны, токсичные вещества (синильная кислота, бензопирен) и др.
В качестве примера в табл. 17.1 представлен удельный выход токсических веществ при горении некоторых материалов.
Таблица 17.1. Удельный выход токсичных газов при горении некоторых материалов
|
Материал |
Наиболее токсичный продукт |
Максимальный выход кг/кг |
|
Ацетохлориновая ткань |
НСl |
0,38* |
|
Винилпласт |
НСl CO |
0,037 0,015 |
|
Волокно ПВХ |
НСl CO |
0,03 0,05 |
|
Декоративно-отделочная пленка |
НСl CO |
0,017 0,15 |
|
Хлопок |
CO CO2 |
0,0052 0,57 |
|
Капрон (волокно) |
НСN |
0.0495* |
|
Кожа искусственная |
НСl CO |
0,006 0,036 |
|
Нитрон (волокно) |
НСN |
0,128* |
|
Древесина |
CO CO2 |
0,024 1.51 |
|
Полистирол |
CO |
0,015 |
|
Фенолформальдегидные полимеры: - лак БЛС; - наволочный СФ-100; - резальный СФ-340 |
CO CO CO |
0,0094 0,009 0,0025 |
|
Хлорин (волокно) при соотношении с целлюлозой в %: - 65/35 - 50/50 - 35/65 |
НСl НСl НСl |
0,392 0,291 0,193 |
* При термоокислительной деструкции
17.2. Основные показатели пожаровзрывоопасности веществ и материалов
Пожаровзрывоопасность веществ и материалов - совокупность свойств, характеризующих их способность к возникновению и распространению горения. Следствием горения, в зависимости от его скорости и условий протекания, может быть пожар (диффузионное горение) или взрыв (дефлаграционное горение предварительно перемешанной смеси горючего с окислителем).
Пожаровзрывоопасность веществ и материалов определяется показателями, выбор которых зависит от агрегатного состояния вещества (материала) и условий его применения.
При определении пожаровзрывоопасности веществ и материалов различают:
- газы - вещества, в которых кинетическая энергия теплового движения молекул значительно превосходит потенциальную энергию взаимодействий между ними;
- жидкости - вещества, давление насыщенных паров которых при температуре 250С и давлении 101,3 кПа меньше 101,3 кПа. К жидкостям относят также твердые плавящиеся вещества, температура плавления и каплепадения которых меньше 500С;
- твердые вещества и материалы ~ индивидуальные вещества и их смесевые композиции с температурой плавления или каплепадения больше 500С, а также вещества, не имеющие температуры плавления (например, древесина, ткани и т.п.);
- пыли - диспергированные твердые вещества и материалы с размером частиц менее 850 мкм.
Показатели пожаровзрывоопасности веществ и материалов выбираются в зависимости от агрегатного состояния (табл. 17.1).
Кроме указанных в табл. 17.2, допускается использовать другие показатели, более детально характеризующие пожаровзрывоопасность веществ и материалов.
Группа горючести является классификационной характеристикой способности веществ и материалов к горению.
По горючести вещества и материалы подразделяются на три группы:
- негорючие (несгораемые) - вещества и материалы, не способные к горению в воздухе. Они могут быть пожаровзрывоопасными, например, окислители или вещества, выделяющие горючие продукты при взаимодействии с водой, кислородом воздуха или друг с другом;
- трудногорючие (трудносгораемые) - вещества и материалы, способные гореть в воздухе при воздействии источника зажигания, но не способные самостоятельно гореть после его удаления;
- горючие (сгораемые) - вещества и материалы, способные самовозгораться, а также возгораться при воздействии источника зажигания и самостоятельно гореть после его удаления.
Таблица 17.2. Номенклатура показателей и их применяемость для характеристики пожаровзрывоопасности веществ и материалов
|
Показатель |
Агрегатное состояние веществ и материалов |
|||
|
Газы |
Жидкости |
Твердые |
Пыли |
|
|
Группа горючести |
+ |
+ |
+ |
+ |
|
Температура вспышки |
- |
+ |
- |
- |
|
Температура воспламенения |
- |
+ |
+ |
+ |
|
Концентрационные пределы распро-странения пламени (воспламенения) |
+ |
+ |
+ |
+ |
|
Температурные пределы распространения пламени (воспламенения) |
+ |
+ |
- |
+ |
|
Температура тления |
- |
+ |
- |
- |
|
Условия теплового самовозгорания |
- |
- |
+ |
+ |
|
Минимальная энергия зажигания |
- |
- |
+ |
+ |
|
Кислородный индекс |
+ |
+ |
- |
+ |
|
Способность взрываться и гореть при взаимодействии с водой, кислородом воздуха и другими веществами |
- |
- |
+ |
- |
|
Нормальная скорость распространения пламени |
+ |
+ |
+ |
+ |
|
Скорость выгорания |
+ |
+ |
- |
- |
|
Коэффициент дымообразования |
+ |
+ |
- |
- |
|
Индекс распространения пламени |
- |
- |
+ |
- |
|
Показатель токсичности продуктов горения полимерных материалов |
- |
- |
+ |
- |
|
Минимальное взрывоопасное содержание кислорода |
- |
+ |
- |
+ |
|
Максимальное давление взрыва |
+ |
+ |
- |
+ |
|
Скорость нарастания давления взрыва |
+ |
+ |
- |
+ |
Примечание. Знак «+» обозначает применяемость, знак «-» - неприменяемость показателя.
Из группы горючих веществ и материалов выделяют легковоспламеняющиеся, которые способны воспламеняться от кратковременного (до 30 с) воздействия источника зажигания с низкой энергией (пламя спички, искра, тлеющая сигарета и т.п.).
Группы горючести используются для оценки веществ и материалов, определения категории помещений по взрывопожарной и пожарной опасности, при разработке мероприятий по пожарной безопасности и др.
Максимальная скорость процесса горения достигается при стехиометрической концентрации, т.е. при концентрации, которая точно соответствует количественному содержанию веществ, соединяемых друг с другом при реакции горения.
Концентрационные пределы распространения пламени нижние или верхние - это минимальное или максимальное содержание горючего вещества в однородной смеси с окислительной средой, при котором возможно распространение пламени по смеси на любое расстояние от источника зажигания.
Концентрационные пределы могут быть выражены через температуру (при атмосферном давлении). Значения температуры жидкости, при которых концентрация насыщенных паров в воздухе над жидкостью равна концентрационным пределам распространения пламени, называются температурными пределами распространения пламени (воспламенения) (нижним и верхним соответственно - НТПРП и ВТПРП).
Интервал между нижним и верхним концентрационными пределами называется областью воспламенения.
Для расчета нижнего и верхнего пределов воспламенения индивидуальных горючих веществ можно использовать следующие эмпирические формулы (в % об.)
НКПРП = 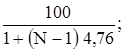 ВКПРП
=
ВКПРП
= 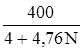 ,
,
где N – число молей – атомов кислорода, участвующих в сгорании 1 моля горючего.
Например. Рассчитать нижний и верхний концентрационные пределы распространения пламени газа и концентрацию газа при аварии, если объем газа, поступившего в помещение при аварии 20 м3. Объем помещения 450 м3. Газ – пропан. Технологическое оборудование занимает 30% объема помещения. Возможен ли при данной концентрации газа и источника воспламенения взрыв газа?
С3Н8+5О2 = 3СО2+4Н2О, N = 5 · 2 = 10
НКПРП = 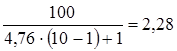 (%
об.)
(%
об.)
ВКПРП = 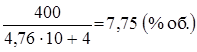
Концентрация пропана при аварии составит
fав. = 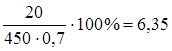 (%
об.)
(%
об.)
При данной концентрации пропана и наличии источника воспламенения взрыв возможен.
Для сложной газовоздушной смеси известного состава пределы воспламенения можно подсчитать по формуле Ле-Шателье (в % об.)
П = 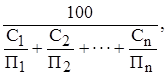
где П – предел воспламенения (нижний и верхний), % об.; С1, С2…Cn – концентрация горючих компонентов в горючей смеси, С2+С2+…+Сn=100 % об.; П1, П2…Пn – соответствующие пределы воспламенения чистых компонентов смеси, % об.
Величины пределов воспламенения используют при расчете допустимых концентраций внутри технологических аппаратов, систем рекуперации, вентиляции, а также при определении предельно допустимой взрывоопасной концентрации (ПДВК) паров и газов при работе с применением искрящего инструмента.
Процесс воспламенения и горения жидкостей можно представить следующим образом. Для воспламенения необходимо, чтобы жидкость была нагрета до определенной температуры (не меньше нижнего температурного предела распространения пламени). После воспламенения паров жидкости скорость испарения должна быть достаточной для поддержания постоянного горения. Эти особенности горения жидкостей характеризуются температурами вспышки и воспламенения.
В соответствии с ГОСТ 12.1.044 температурой вспышки называется наименьшая температура конденсированного вещества, при которой в условиях специальных испытаний над его поверхностью образуются пары, способные вспыхивать в воздухе от источника зажигания; устойчивое горение при этом не возникает. Температура вспышки соответствует нижнему температурному пределу воспламенения.
Температуру вспышки используют для оценки воспламеняемости жидкости, а также при разработке мероприятий для обеспечения пожаро- и взрывобезопасности ведения технологических процессов.
В зависимости от численного значения температуры вспышки жидкости подразделяются на легковоспламеняющиеся (ЛВЖ) и горючие (ГЖ).
К легковоспламеняющимся относятся жидкости с температурой вспышки не более 610С в закрытом тигле или 660С в открытом тигле. Для ЛВЖ температура воспламенения обычно на 1-50С выше температуры вспышки, а для горючих жидкостей эта разница может достигать 30-35°С.
В соответствии с ГОСТ 12.1.017, в зависимости от температуры вспышки ЛВЖ подразделяются на три разряда.
Особо опасные ЛВЖ — с температурой вспышки от -180С и ниже в закрытом тигле или от -13°С и ниже в открытом тигле. К особо опасным ЛВЖ относятся ацетон, диэтиловый спирт, изопентан и др.
Постоянно опасные ЛВЖ - это горючие жидкости с температурой вспышки от -180С до +230С в закрытом тигле или от -130С до +270С в открытом тигле. К ним относятся бензин, толуол, этиловый спирт, этилацетат и др.
Опасные при повышенной температуре ЛВЖ - это горючие жидкости с температурой вспышки от 23 до 610С в закрытом тигле. К ним относятся хлорбензол, скипидар, уайт-спирит и др.
Температура вспышки жидкостей, принадлежащих к одному классу (жидкие углеводороды, спирты и др.), закономерно изменяется в гомологическом ряду, повышаясь с увеличением молекулярной массы, температуры кипения и плотности.
Температуру вспышки определяют экспериментальным и расчетным путями. Для экспериментального определения температуры вспышки заданную массу жидкости (вещества) нагревают с определенной скоростью, периодически зажигая выделяющиеся пары и визуально оценивая результаты зажигания.
Ориентировочно расчет температуры вспышки (tвсп) можно получить из уравнения Элея, 0С
tвсп = tкип - 18 ![]() ,
,
где tкип - температура кипения, 0С;
К – коэффициент горючести, величина которого находится из алгебраической суммы произведения числа атомов, входящих в состав молекул на соответствующий коэффициент.
К = 4С + 4S + 1H + 1N – 20 – 2Cl – 3F – 5Вr ,
если К > 2 – вещество горючее;
К = 0+2 – трудногорючее;
К < 0 – негорючее.
Температурой воспламенения называется наименьшее значение температуры жидкости, при котором интенсивность испарения ее такова, что после зажигания внешним источником возникает самостоятельное пламенное горение.
Температура самовоспламенения - самая низкая температура вещества, при которой в условиях специальных испытаний происходит резкое увеличение скорости экзотерических реакций, заканчивающихся горением.
Минимальное взрывоопасное содержание кислорода (окислителя) - такая его концентрация в горючей смеси, ниже которой воспламенение и горение смеси становятся невозможными при любой концентрации горючего в смеси, разбавленной данным флегматизатором.
Склонность к взрыву и детонации - чувствительность к механическому воздействию (удару или трению).
Взрывоопасной средой являются: смеси веществ (газов, паров, пылей) с воздухом и другими окислителями (кислород, озон, хлор, окислы азота и др.), способные к взрывчатому превращению, а также индивидуальные вещества, склонные к взрывному разложению (ацетилен, озон, гидразин, аммиачная селитра и др.).
Основными параметрами, характеризующими опасность взрыва, являются:
- максимальное давление взрыва — наибольшее давление, возникающее при дефлаграционном взрыве газо-, паро- или пылевоздушной смеси в замкнутом сосуде при начальном давлении смеси 101,3 кПа;
- скорость нарастания давления при взрыве — это производная давления взрыва по времени на восходящем участке зависимости давления взрыва газо-, паро-, пылевоздушной смеси в замкнутом сосуде от времени.
Минимальная энергия зажигания— наименьшее значение энергии электрического разряда, способного воспламенить наиболее легко воспламеняющуюся смесь газа, пара или пыли с воздухом. Для ориентировочного расчета минимальной энергии зажигания паров и газов в воздухе Emin, мДж, применяется формула
Emin =
0,049![]() ,
,
где dкр - критический зазор, величину которого можно получить расчетным путем или на основе справочных данных, мм.
Для оценки взрывоопасности газо- и паровоздушных смесей используют понятие критического зазора (диаметра).
С критическим диаметром (зазором) связано также определение категории взрывоопасной смеси, которая характеризует способность газопаровоздушной смеси передавать взрыв через узкие щели и фланцевые зазоры.
В соответствии с ГОСТ 30852.11-2002 взрывоопасные смеси газов и паров подразделяются на категории взрывоопасности в зависимости от величины безопасного экспериментального максимального зазора (БЭМЗ) и значения соотношения минимального тока воспламенения испытуемого газа или пара к минимальному току воспламенения метана (МТБ).
БЭМЗ - это экспериментальный максимальный зазор, через который не происходит передача взрыва из оболочки в окружающую среду при любой концентрации горючего в воздухе (рис. 17.1).
Установлены два вида взрывоопасных смесей: I - метан на подземных горных работах; II - газы и пары, за исключением метана на подземных горных работах.
В зависимости от значений БЭМЗ и МТВ газы и пары подразделяются на категории (табл. 17.3).
Таблица 17.3. Категории взрывоопасности смесей в зависимости
от величины БЭМЗ и МТВ
|
Категория взрывоопасности смесей |
Величина БЭМЗ, мм |
Величина МТВ |
|
II А |
0,9 и более |
более 0,8 |
|
II В |
свыше 0,5, но менее 0,9 |
от 0,4 до 0,8 вкл |
|
II С |
0,5 и менее |
менее 0,45 |
Для классификации большинства газов и паров достаточно применения одного из критериев - значения БЭМЗ или МТВ.
Один критерий достаточен в следующих случаях:
- для категории ПА - БЭМЗ больше 0,9 мм или соотношение МТВ больше 0,9;
- для категории ПВ - БЭМЗ в 0,5 до 0,8;
- для категории ПС - БЭМЗ меньше 0,5 мм или соотношение МТВ меньше 0,45.
Необходимо определять как БЭМЗ, так и соотношение МТВ в следующих случаях:
- если установлено только соотношение МТВ и его значение находится в пределах от 0,45 до 0,5 или от 0,8 до 0,9;
- если известен только БЭМЗ и его значение находится в пределах от 0,5 до 0,55.
Кроме категорий взрывоопасные смеси газов и паров подразделяются на группы в зависимости от величины температуры самовоспламенения согласно таблица 17.4.
Таблица 17.4. Классификация взрывоопасных смесей
по температуре самовоспламенения
|
Группа взрывоопасных смесей |
Температура самовоспламенения, °С |
|
Т1 |
Свыше 450 |
|
Т2 |
Свыше 300 до 450 включительно |
|
ТЗ |
Свыше 200 до 300 включительно |
|
Т4 |
Свыше 135 до 200 включительно |
|
Т5 |
Свыше 100 до 135 включительно |
|
Т6 |
Свыше 85 до 100 включительно |
Характеристика взрывоопасных смесей необходима для обоснованного выбора электрооборудования для взрыво- и пожароопасных производственных помещений и наружных установок.
Самовозгорание - резкое увеличение скорости экзотермических процессов в веществе, приводящее к возникновению очага горения. Оно является результатом самонагревания веществ, заканчивающегося тлением или пламенным горением. Процесс самонагревания веществ может быть вызван различными причинами. Это могут быть микробиологические процессы в соответствующей питательной среде, воздействие высокой температуры на вещество, выделение тепла в результате химических реакций.
Микробиологические процессы окисления - основная причина самовозгорания веществ растительного происхождения, например, недосушенных сена, опилок, листьев.
Микробиологическими же процессами объясняется самовозгорание фрезерного торфа, жизнедеятельность бактерий и грибков в котором может начаться уже при 10-18°С и заканчивается при 70 °С. Питательной средой для бактерий служат водорастворимые вещества, образующиеся в результате распада растений.
Тепловое самовозгорание присуще дисперсным веществам, обладающим сильно развитой поверхностью, способным адсорбировать кислород и вступать с ним в реакцию, а теплообмен веществ с внешней средой не является интенсивным.
Так, к самовозгоранию склонны ископаемые угли (бурый и каменный), хранящиеся в кучах или штабелях. Причины самовозгорания - способность углей окисляться и адсорбировать пары и газы при низких температурах.
Самовозгоранию углей способствует степень их измельчения, а также наличие в них примесей - пирита и влаги.
При химическом самовозгорании большое значение имеет скорость химической реакции. Недостаточный теплоотвод способствует нагреву материала в результате окислительных процессов и соответственно достижению критических условий возникновения горения или тления.
Самовозгорающиеся химические вещества можно разделить на три основные группы.
1. Вещества, самовозгорающиеся при взаимодействии с воздухом.
Щелочные металлы (литий, натрий, калий, рубидий, цезий), окисляясь на воздухе, самовозгораются с образованием надпероксидов металлов.
К + О2 → КО2 +283,8 кДж.
Сульфиды щелочных (например, калия) и щелочноземельных металлов (например, кальция) окисляясь на воздухе могут самовозгораться. Гидроксиды металлов с кислородом воздуха образуют пероксиды водорода. Негорючий гидросульфит натрия в этих условиях образует серу, способную к воспламенению. К характерным представителям этой группы относятся белый и красный фосфор. Легко самовозгораются на воздухе, особенно в присутствии влаги, аэрогели алюминия и цинка. Взрывчатые смеси образуют на воздухе алюминиевая и магниевая пудра. Диэтиловый эфир способен самовозгораться на воздухе, что связано с образованием пероксидов.
Самовозгорание олиф, растительных масел (льняного, подсолнечного и др.) связано с их химическим строением, так как они представляют собой смесь глицеридов жирных кислот, в том числе и непредельных — олеиновой, линолевой, линоленовой. Наличие в молекулах двойных связей и является причиной окисления указанных кислот при обычных температурах. Кроме того, самовозгоранию способствует полимеризация глицеридов непредельных кислот - экзотермический процесс, происходящий при низких температурах.
В связи со способностью масел и жиров самовозгораться большую опасность представляют промасленная одежда и обтирочные материалы, загрязненные растительными маслами. При большой поверхности загрязнения, на которой масло распределено тонким слоем, резко ускоряются реакции окисления и полимеризации. Подобные процессы нагревания начинаются уже при 10-150С и, продолжаясь несколько часов, заканчиваются самовозгоранием.
2. Вещества, самовозгорающиеся при взаимодействии с водой.
К этой группе относятся щелочные металлы, карбиды щелочных металлов, карбид кальция, гидриды щелочных и щелочноземельных металлов, негашеная известь, фосфористый кальций, сернистый натрий и другие, т.е. вещества, взаимодействие которых с водой сопровождается значительным экзотермическим эффектом. Образующейся при этом теплоты достаточно, чтобы вызвать воспламенение выделяющихся в результате реакции горючих соединений.
Контакт негашеной извести с небольшим количеством воды сопровождается выделением значительного количества теплоты, которой может быть достаточно для воспламенения дерева.
3. Вещества, самовозгорающиеся при взаимодействии друг с другом.
Источниками кислорода в условиях пожара могут быть твердые и жидкие окислители, например, пероксиды водорода, натрия, калия, хлораты и перхлораты, нитраты и др. Значительный экзотермический эффект, сопровождающий разложение пероксида водорода, вызывает интенсивный разогрев парогазовой смеси.
Пероксид водорода разлагается диоксидом марганца, хрома, цинка. В присутствии концентрированного пероксида водорода спирты, кетоны, ароматические углеводороды и другие самовозгораются, либо становятся чувствительными к нагреванию.
Концентрированная азотная кислота вызывает самовозгорание многих горючих веществ. В присутствии серной кислоты ее окисляющее действие усиливается. Концентрированная азотная кислота при взаимодействии с многими металлами восстанавливается до диоксида азота, разбавленная HNO3 — до оксинитрида азота, которые в свою очередь химически активны.
Известно, что продукты взаимодействия азотной кислоты с органическими веществами обладают более пожароопасными свойствами. Например, взаимодействие азотной кислоты с гликолями и глицеринами приводит к образованию взрывчатых веществ — сложных эфиров.
Сильным окислителем является серная кислота. Разбавленная H2SO4 растворяет металлы и при этом выделяется водород, а взаимодействие ее с щелочными и щелочноземельными металлами сопровождается самовозгоранием. Концентрированная H2SO4, взаимодействуя с металлами, может образовывать диоксид серы, серу, сульфид водорода. Большая часть органических веществ в присутствии H2SO4 обугливается. Присутствие H2SO4 усиливает пожароопасные свойства таких окислителей, как перманганат калия, хлорат калия, нитраты и др.
Сильными газообразными окислителями являются F2, O2, Вг2 и ряд их соединений. Фтор вызывает самовозгорание всех органических веществ. При нагревании во фторе горят практически все металлы, песок, стеклянная вата, асбест, бетон. В среде фтора самовозгораются бром, йод, сера, теллур, фосфор, мышьяк, сурьма, щелочные и щелочноземельные металлы и др.
В атмосфере хлора горят многие органические веществу, металлы и др. При взаимодействии хлора с органическими жидкостями выделение большого количества тепла способствует испарению жидкости и образованию взрывоопасных смесей. Жидкий хлор более опасен, чем газообразный. Бром уступает по активности фтору и хлору. Пары брома вызывают самовозгорание некоторых органических веществ.
К неорганическим окислителям относятся перхлораты, хлораты, нитраты, перманганаты, дихроматы, хроматы, гипохлориты натрия, калия, кальция, пероксиды и надпероксиды многие другие химические соединения.
Контрольные вопросы
1. Охарактеризуйте условия и виды процесса горения?
2. Какие различают основные показатели пожаровзрывоопасности веществ и материалов?
3. Что такое взрыв, его физико-химическая сущность?
4. Что такое температуры вспышки и воспламенения веществ, методы их расчета?
5. Какая практическая значимость температурных и концентрационных пределов распространения пламени?
6. Какова физико-химическая сущность самовозгорания?



